電極を外部電源に接続すると、電気回路が形成されます。電解セル装置内の陽極電極は外部電源の正極に接続され、陰極電極は外部電源の負極に接続されます。たとえば、水を電気分解して水素と酸素を生成する場合、電子の流れ方向は外部電源の負極から電解セルの陰極、電解セルの陽極、外部電源の正極の順ですが、電流の流れ方向は正反対です(電子は負の電荷を持っています)。そのため、電解セルの陰極材料上でH+還元反応(つまりHERプロセス)が発生してH2が生成され、電解セルの陽極材料上で電解水中に水素と酸素を生成する酸化反応(つまりOER)が発生してO2が生成されます。電解セル全体の作業効率を確保するために、電解セルの電極材料には、良好な電子伝達導電性を持ち、対応する酸化還元反応を触媒できるという要件があります。
HER は、電気触媒による水分解中に陰極に作用する反応です。1905 年にターフェルが発見しました。酸性媒体中の金属表面での水素発生反応は次のとおりです。

アルカリ性または中性媒体の場合:

上記の反応において、Mは電極の金属材料であり、水の電気分解における水素と酸素の生成プロセスは、金属Mに吸着された水素です。ボルマー反応は水素吸着ステップと呼ばれ、ヘイロフスキー反応は電気化学的脱着ステップと呼ばれ、ターフェル反応は化学的脱着ステップ(吸着から電気化学的脱着、化学的脱着プロセス)と呼ばれます。水素発生反応は、典型的な中間生成物触媒二重電子移動反応です。外部電位の駆動により、電極は電解質から活性水素と酸素生成を得て水を電気分解します。その後、吸着された原子は脱着プロセスを通じて結合し、水素を生成します。前の式の分析により、異なる電解媒体で発生する反応メカニズムと経路が異なることがわかります。いずれにせよ、HERの進化は3つの基本的なステップを経てきました。
a) ボルマー反応:このプロセスは電子移動プロセスであり、電気化学プロセスとも呼ばれます。一般的に、酸性電解質では、H +が電子を獲得して電解水中に水素と酸素を生成します。アルカリ電解質では、H2Oが電子になることができます。水の電気分解における水素と酸素の生成プロセスと、水の電気分解における水素と酸素の生成プロセスは、酸性電解質で簡単に確認できます。ボルマー反応は、水分子の抵抗を克服する必要がなく、エネルギー障壁を突破します。したがって、アルカリ電解質と比較して、酸性条件下ではHERプロセスがより簡単に発生します。
(b)ヘイロフスキー:これは電気化学的脱着プロセスと呼ばれています。水中の水素と酸素の電気分解、および電解質中のH+またはH2Oの電気分解によって生成された陽子が電子を獲得してH2分子を形成し、その後脱着して沈殿するプロセスです。
(c) ターフェル反応:複合脱着プロセスと呼ばれ、簡単に言えば、水の電気分解によって生成された水素と酸素がアルカリ性電解質と酸性電解質中のH2に変換されるプロセスです。
完全な HER プロセスには電気化学プロセスと 1 ステップの脱着プロセスが含まれるため、HER の電気触媒は通常、Volmer-Heyrovsky または Volmer-Tafel メカニズムとして説明されます。これらの 3 つの反応ステップは HER 反応の決定的なプロセスである可能性があり、反応の動的プロセスは一般に HER 分極曲線の Tafel 勾配によって決定されます。
低速放電理論は、電気化学反応段階(Volmer 反応)が決定的な段階であるという観察に基づいています。電気化学的脱着理論は、電気化学脱着段階(Heyrovsky 反応)が決定的な段階であるという観察に基づいています。混合理論によると、決定的な段階は複雑な脱着段階(Heyrovsky-Tafel 反応)です。
さらに分析すると、水素発生反応では、まず反応粒子が一定の力で触媒表面に吸着して反応中間体を形成し(M-電解水中の水素と酸素の生成過程)、次にM-電解水中の水素と酸素の生成過程で結合が切断され、H2が生成される。したがって、水素吸着の自由エネルギーΔGHは、水素発生反応の全体速度にとって決定的である。明らかに、電極の吸着能力は触媒の役割に直接関係している。弱い吸着の場合、Volmer反応は抑制されるため、律速段階はVolmer自体である。触媒の強い作用により、M-電解水中の水素と酸素生成過程の結合が切断され、H2が形成されると、反応の脱着過程(Heyrovsky-Tafel)が決定的過程となる。したがって、水素発生触媒の場合、触媒表面の水素吸着の自由エネルギーΔGH≈0が最適であると一般に考えられている。
触媒活性を促進するもう一つの重要な要素は電流密度です。実際、HER 交換電流密度と吸着水素の自由エネルギーの関係は以下のように表されます。

触媒自由エネルギーによる電流密度の変化
この図は、サバティエ原理と呼ばれるさまざまな金属の触媒活性を表しています。この原理は、触媒の触媒特性を定量的に説明するために使用でき、HER 触媒の設計とスクリーニングのための重要なツールの 1 つです。
OER は、材料の組成、結晶構造、表面特性、形状など、多くのパラメータに依存するプロセスです。一般的に、反応メカニズムは 4 電子移動プロセスであると考えられており、O2 を生成するには 4 段階の酸化還元反応が必要です。このため、OER は HER に比べて遅くなります。したがって、これが電気分解ユニットの全体的なパフォーマンスを決定する制限要因となります。実際、水電気分解の全体的な開発では、陽極は陰極に比べて高い過電圧を持つ必要があります。
4 つの電子の挙動を考慮すると、OER は HER よりも複雑です。電気分解セル (スタック) で使用されるさまざまな触媒の OER メカニズムも異なります。酸性媒体で認識されている主な酸素発生反応は次のとおりです。

M は触媒活性部位であり、酸素沈殿の場合、最初の 2 つの式と最後の 2 つの式は平行しています。酸性媒体では、貴金属 (Ir、Ru およびそれらの酸化物) が触媒として使用されますが、他の金属は腐食プロセスが速いため、触媒としては適していません。アルカリ性または中性媒体では、反応は次のように進行します。
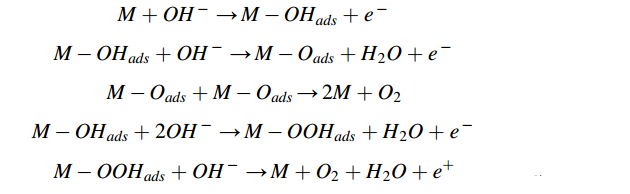
酸性媒体との主な違いは、水酸化物イオンの吸着です。触媒表面に形成されたヒドロキシル基は吸着酸素アニオンを形成し、さらに別のOH-の脱プロトン化により放出されて酸素原子を形成します。また、最後の2つの式は、M-OH結合がOH結合と切断されて過酸化物を形成し、それが分解して酸素を生成することを示しています。上記の反応における電荷移動ステップは決定的な速度ステップですが、異なる材料と異なる反応条件では、決定的な速度ステップが異なり、ターフェル勾配の大きさに応じて識別できます。科学者は、遷移金属酸化物、ペロブスカイト材料、炭素ベースの非金属材料など、貴金属材料に代わるさまざまな効率的で安定したOER電極触媒を開発しました。その中でも、ペロブスカイトは、その複雑で制御可能な電子構造により、広く使用されるOER電極触媒となっています。
